metaalkarakter
Atomen proberen naar een stabielere elektronenbetting te evolueren door een of meer elektronen op te nemen of af te geven. Hierin onderscheiden we metalen en niet-metalen.
Een parameter voor het metaal-karakter is de elektronegativiteit = maat voor de neiging van een atoom dat een chemische binding aangaat met een buuratoom om de gezamenlijke elektronenwolk naar zich toe te trekken.
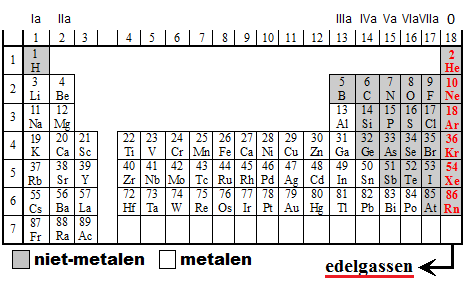
metalen en niet-metalen
| metalen | niet-metalen |
| - neiging tot afstaan van elektronen | - neiging tot opnemen van elektronen |
| - vorming van positieve ionen | - vorming van negatieve ionen |
| - elektropositief karakter | - elektronegatief karakter |
| - lage EN-waarde | - hoge EN-waarde |
- de atomen helemaal links in het PSE maar weinig elektronen afgeven voor een octetconfiguratie
- de atomen helemaal rechts in het PSE maar weinig elektronen opgeven voor een octetconfiguratie
Elektronegativiteit
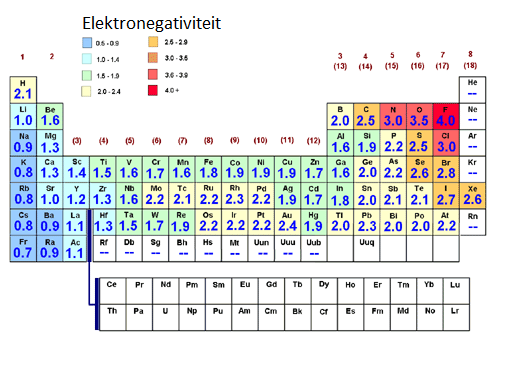
- De elementen linksonder in het PSE hebben het sterkste metaalkarakter (de laagste EN-waarde)
- De elementen rechtsboven in het PSE hebben het zwakste metaalkarakter (de hoogste EN-waarde)